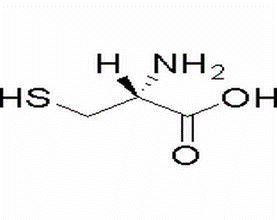
แอล-ซิสเทอีน (CAS# 52-90-4)
| สัญลักษณ์อันตราย | Xn – เป็นอันตราย |
| รหัสความเสี่ยง | R22 – เป็นอันตรายหากกลืนกิน R36/37/38 – ระคายเคืองต่อดวงตา ระบบทางเดินหายใจ และผิวหนัง. |
| คำอธิบายด้านความปลอดภัย | S26 – ในกรณีที่เข้าตา ให้ล้างออกด้วยน้ำปริมาณมากทันทีและไปพบแพทย์ S37/39 – สวมถุงมือและอุปกรณ์ป้องกันตา/ใบหน้าที่เหมาะสม |
การแนะนำ
L-cysteine (L-Cysteine) เป็นกรดอะมิโนที่ไม่จำเป็นซึ่งเข้ารหัสโดย codons UGU และ UGC และเป็นกรดอะมิโนที่ประกอบด้วยซัลไฮดริล เนื่องจากมีหมู่ซัลไฮดริล ความเป็นพิษจึงมีน้อย และในฐานะสารต้านอนุมูลอิสระ จึงสามารถป้องกันการเกิดอนุมูลอิสระได้ & & L-cysteine เป็นกรดอะมิโนที่ไม่จำเป็นที่เกิดขึ้นตามธรรมชาติ เขาเป็นนักเคลื่อนไหวของ NMDA นอกจากนี้ยังมีบทบาทหลายอย่างในการเพาะเลี้ยงเซลล์ ดังนี้ 1. สารตั้งต้นในการสังเคราะห์โปรตีน; หมู่ซัลไฟด์ริลในซิสเทอีนมีบทบาทสำคัญในการก่อตัวของพันธะไดซัลไฟด์ และยังรับผิดชอบในการพับโปรตีน การสร้างโครงสร้างทุติยภูมิและตติยภูมิ 2. การสังเคราะห์ Acetyl-CoA; 3. ปกป้องเซลล์จากความเครียดจากปฏิกิริยาออกซิเดชั่น 4. เป็นแหล่งกำมะถันหลักในการเพาะเลี้ยงเซลล์ 5. ไอโอโนฟอร์โลหะ & & กิจกรรมทางชีวภาพ: Cysteine เป็นกรดα-อะมิโนที่มีขั้วซึ่งมีหมู่ซัลไฮดริลอยู่ในกลุ่มอะลิฟาติก ซีสเตอีนเป็นกรดอะมิโนจำเป็นตามเงื่อนไขและกรดอะมิโนแซ็กคาโรเจนิกสำหรับร่างกายมนุษย์ สามารถเปลี่ยนจากเมไทโอนีน (เมไทโอนีนซึ่งเป็นกรดอะมิโนที่จำเป็นสำหรับร่างกายมนุษย์) และสามารถแปลงเป็นซีสตีนได้ การสลายตัวของซิสเทอีนจะถูกสลายตัวเป็นไพรูเวต ไฮโดรเจนซัลไฟด์ และแอมโมเนียโดยผ่านการกระทำของเดสซัลฟูเรสภายใต้สภาวะไร้ออกซิเจน หรือผ่านการทรานอะมิเนชัน ผลิตภัณฑ์ระดับกลาง β-mercaptopyruvate จะถูกสลายตัวเป็นไพรูเวตและซัลเฟอร์ ภายใต้สภาวะออกซิเดชัน หลังจากถูกออกซิไดซ์เป็นกรดซิสเตอีนซัลฟิวรัส มันสามารถสลายตัวเป็นกรดไพรูเวตและกรดซัลฟูรัสได้โดยการทรานอะมิเนชัน และสลายตัวเป็นทอรีนและทอรีนโดยดีคาร์บอกซิเลชัน นอกจากนี้ซิสเทอีนยังเป็นสารประกอบที่ไม่เสถียร รีดอกซ์ได้ง่าย และสลับกับซีสตีน นอกจากนี้ยังสามารถควบแน่นด้วยสารประกอบอะโรมาติกที่เป็นพิษเพื่อสังเคราะห์กรดเมอร์แคปทูริกเพื่อล้างพิษ ซิสเทอีนเป็นสารรีดิวซ์ซึ่งสามารถส่งเสริมการสร้างกลูเตน ลดเวลาที่ต้องใช้ในการผสม และลดพลังงานที่จำเป็นสำหรับการใช้ยา ซิสเตอีนทำให้โครงสร้างของโปรตีนอ่อนลงโดยการเปลี่ยนพันธะไดซัลไฟด์ระหว่างโมเลกุลโปรตีนและภายในโมเลกุลโปรตีน เพื่อให้โปรตีนยืดออก